بازدید و بهره برداری از واحد بازیافت زیستی پسماند غذایی، شرکت رها زیست تولید
/در News and Events /توسط rahazistدر تاریخ ۱۷ بهمن ماه ۱۴۰۲، آقای قلندر شریف شهردار و اعضای شورای شهر مشهد، آقای دکتر طهوری مشاور فناوری وزیر کشور به همراه مدیرعامل محترم سازمان مدیریت پسماند شهرداری مشهد از بزرگترین واحد بازیافت زیستی پسماند غذایی (فارم پرورش میل ورم) شرکت رها زیست تولید واقع در مجتمع بازیافت شهرداری مشهد بازدید بعمل آوردند.
شرکت رها زیست تولید از سال ۹۸ بعنوان پیشران در زمینه توسعه اقتصاد دانش بنیان و تبدیل پسماندهای صنفی وکشاورزی به خوراک دام، طیور و آبزیان فعالیت دارد.



برگزاری نمایشگاه دستاوردهای فناورانه در حوزه اقتصاد چرخشی
/در News and Events /توسط adminبرگزاری نمایشگاه دستاوردهای فناورانه در حوزه اقتصاد چرخشی


نخستین رویداد ملی، دموی کاربرد فناوری در اقتصاد چرخشی با رویکرد صنایع غذایی
/در News and Events /توسط adminنخستین رویداد ملی، دموی کاربرد فناوری در اقتصاد چرخشی با رویکرد صنایع غذایی
بیست و دومین نمایشگاه بین المللی دام، طیور و صنایع وابسته
/در News and Events /توسط rahazistاین نمایشگاه که در تاریخ ۱ تا ۴ مرداد ماه سال ۱۴۰۲ در محل نمایشگاه های بین المللی تهران دائر است. شایان ذکر است شرکت های مربوطه شامل تولیدکنندگان و تامین کنندگان خوراک دام و طیور ، ماشین آلات و صنایع وابسته به آن مشارکت داشتند.
نمایشگاه ایران آگروفود، سی امین نمایشگاه بین المللی تخصصی صنایع کشاورزی، مواد غذایی، ماشین آلات و صنایع وابسته تهران سال ۱۴۰۲
/در News and Events /توسط rahazistبازدید از قدیمی ترین نمایشگاه در صنعت مواد غذایی کشور با جذب بیش از ۱۵۰۰ مشارکت کننده و ۴۰۰۰۰ بازدید کننده بزرگترین نمایشگاه صنایع غذایی در منطقه پس از گلفود دبی است. این نمایشگاه توسط سالیانه برگزار می شود. کلیه شرکت های تولید کننده مواد غذایی، آشامیدنی ها، مواد اولیه صنعت غذا، ماشین آلات صنایع غذایی در این نمایشگاه بزرگ شرکت داشتند.
دستاوردهای رها زیست در نمایشگاه بین المللی مدیریت پسماند و بازیافت، ماشین آلات و تجهیزات وابسته
/در News and Events /توسط rahazistحضور هلدینگ لیدکو در غرفه 15 این نمایشگاه، دستاوردهای بسیار مفید و موثری را همراه داشت. شرکت رها زیست با رویکرد جدید در اقتصاد چرخشی و امنیت غذایی مورد استقبال قرار گرفت. تعامل با موسسات و دیگر شرکتهای دانش بنیان در این حوزه موجبات گام جدیدی برای این هلدینگ خواهد شد. در مکان نمایشگاه نیز با شرکتهای سازنده و طراح ماشین آلات مکانیزه رایزنی صورت گرفت. از شهرداری استان های مختلف در خواست همکاری دو جانبه انجام شد.

دستیابی به دانش تبدیل پسماند به مواد ارزشمند بر پایه اقتصاد چرخشی توسط تیم رها زیست
/0 دیدگاه /در News and Events /توسط rahazist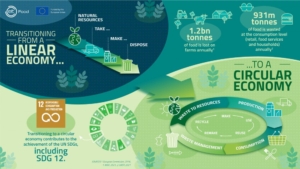
ارائه راهکار جهت افزایش بهره وری میزان تولید توسط تیم رها زیست
/0 دیدگاه /در News and Events /توسط rahazist
بهینه سازی صفر تا صد فرآیند های تولید و پرورش حشرات مفید
/0 دیدگاه /در News and Events /توسط rahazist











